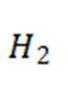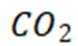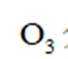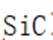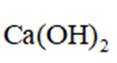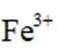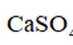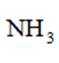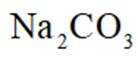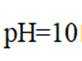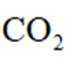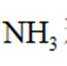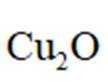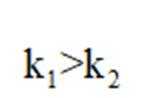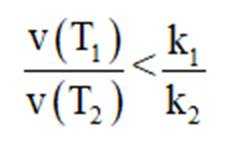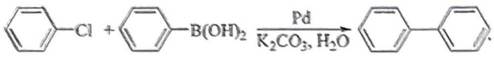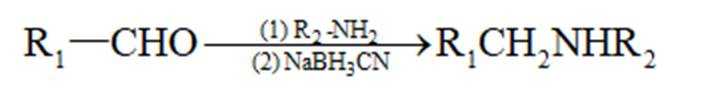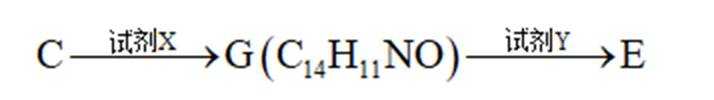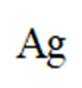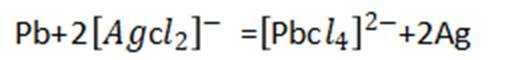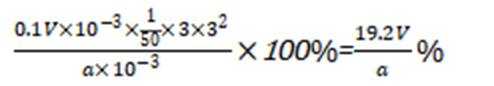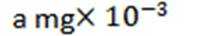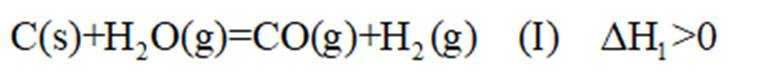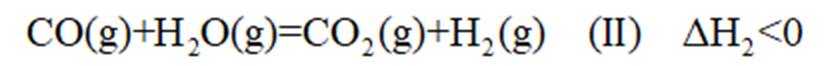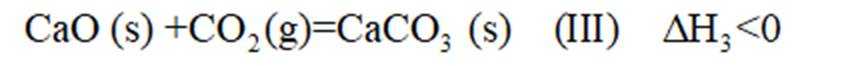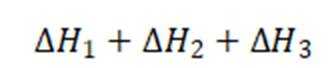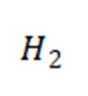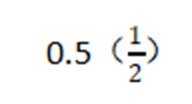- 真题试卷
- 模拟试卷
- 预测试卷
中国书画是世界艺术瑰宝,古人所用文房四宝制作过程中发生氧化还原反应的是( )
正确答案
解析
松木有机物中碳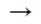
化学品在食品工业中也有重要应用,下列说法错误的是( )
正确答案
解析
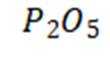
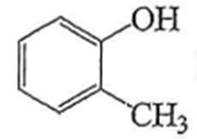
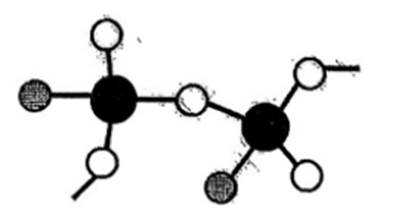
下列化学用语或图示正确的是( )
正确答案
解析
B中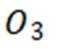
下列物质均为共价晶体且成键结构相似,其中熔点最低的是( )
正确答案
解析
都是共价晶体 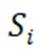
物质性质决定用途,下列两者对应关系错误的是( )
正确答案
解析
电解质使胶体聚沉
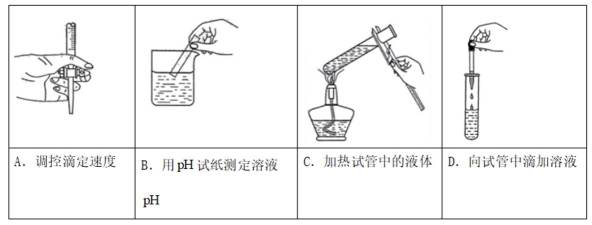
下列图示实验中,操作规范的是( )
正确答案
解析
B中玻璃棒蘸取滴试纤 C中液体过多,应用外焰 D中不能伸进试管
我国科学家在青蒿素研究方面为人类健康作出了巨大贡献。在青蒿素研究实验中,下列叙述错误的是( )
正确答案
解析
核磁共振谱鉴别机构
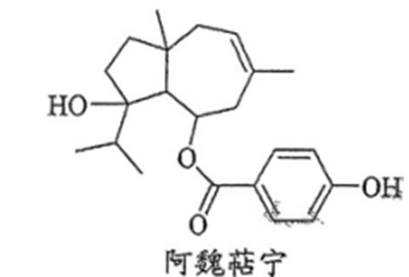
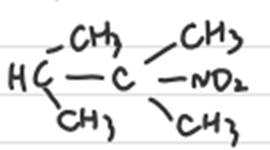
植物提取物阿魏萜宁具有抗菌活性,其结构简式如图所示。下列关于阿魏萜宁的说法错误的是( )
正确答案
解析
消去反应产物最多3种 连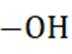
由O,F,I组成化学式为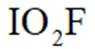
正确答案
解析



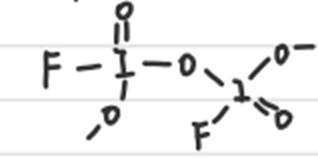
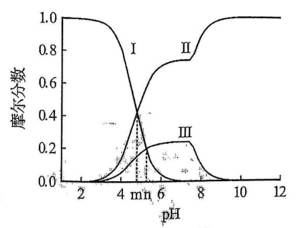
常温下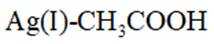
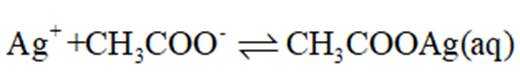
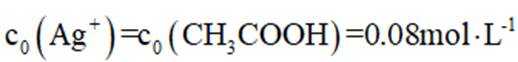
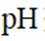
正确答案
解析
A中Ⅱ是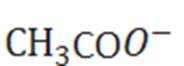
中国美食享誉世界,东坡诗句“芽姜紫醋炙银鱼”描述了古人烹饪时对食醋的妙用。食醋风味形成的关键是发酵,包括淀粉水解、发酵制醇和发酵制酸等三个阶段。下列说法错误的是( )
正确答案
解析
c中制得酸和原来的醇可生成酯
以不同材料修饰的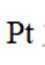
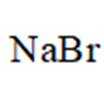
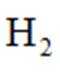
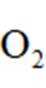
正确答案
解析
B中补充
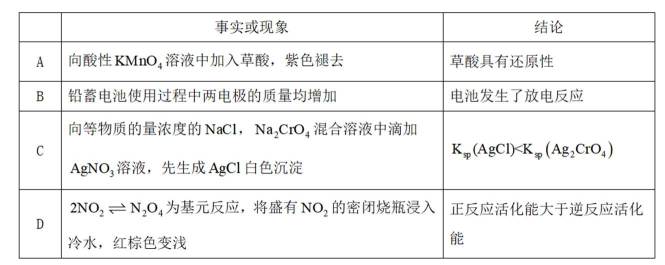
由下列事实或现象能得出相应结论的是( )
正确答案
解析
C中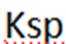
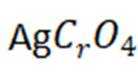
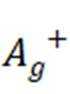
钧瓷是宋代五大名瓷之一,其中红色钩瓷的发色剂为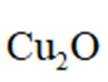
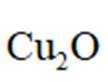
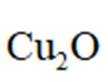
正确答案
解析
B中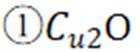
逆水气变换反应: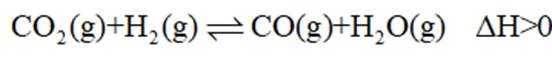
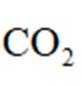
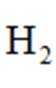
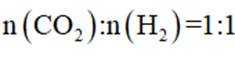
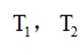
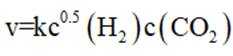
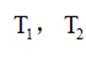
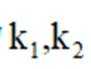
正确答案
解析
C中增大压强c变大v变大
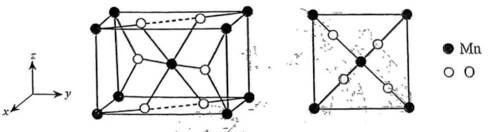
(12分)锰氧化物具有较大应用价值,回答下列问题:
(1)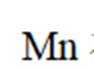
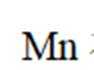
(2)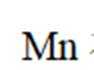
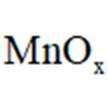
当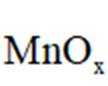
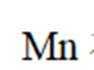
删除A.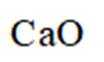
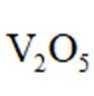
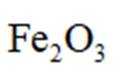
(3)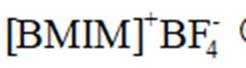
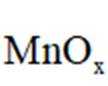
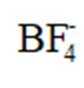
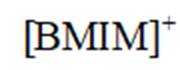
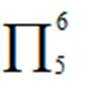
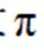
(4)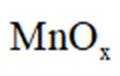
正确答案
(1)四 VⅡB
(2)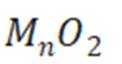
(3)正四面体形
(4)形成更多分子间氢键
解析
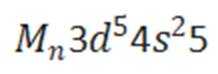
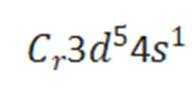
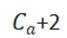
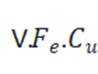
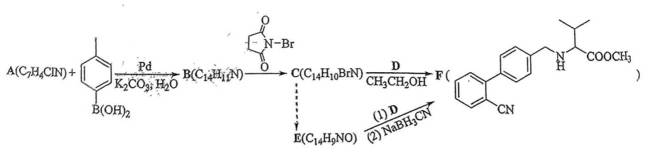
(12分)心血管药物缬沙坦中间体(F)的两条合成路线如下:
已知:
I.
II.
回答下列问题:
(1)A结构简式为_________;B→C反应类型为__________________。
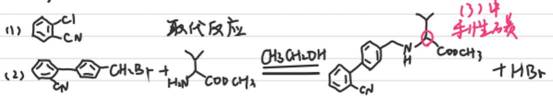
(2)C+D→F化学方程式为___________________________。
(3)E中含氧官能团名称为__________________;F中手性碳原子有_________个。
(4)D的一种同分异构体含硝基和3种不同化学环境的氢原子(个数此为6:6:1),其结构简式为__________________。
(5)C→E的合成路线设计如下:
试剂X为__________________(填化学式);试剂Y不能选用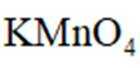
正确答案
(3)醛基 1
(4)
(5)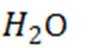
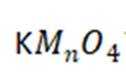
解析
(3)中手性碳
(5)卤代烃水解
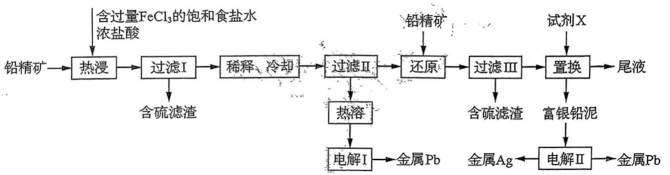
(12分)以铅精矿(含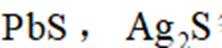
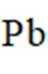
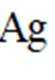
回答下列问题:
(1)“热浸”时,难溶的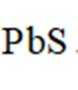
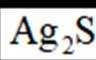
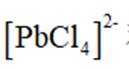
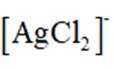
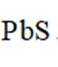
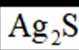
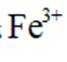
(2)将“过滤Ⅱ”得到的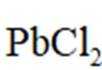
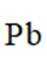
(3)“还原”中加入铅精矿的目的是__________________。
(4)“置换”中可选用的试剂X为_________(填标号)
A.
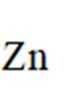
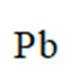
“置换”反应的离子方程式为__________________。
(5)“电解II”中将富银铅泥制成电极板,用作_________(填“阴极”或“阳极”)。
正确答案
(1)1:1
(2)热浸
(3)将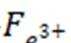
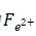
(4)C
(5)阴极
解析
将二价Pb变为Pb单质.最终得Pb.Ag单质.
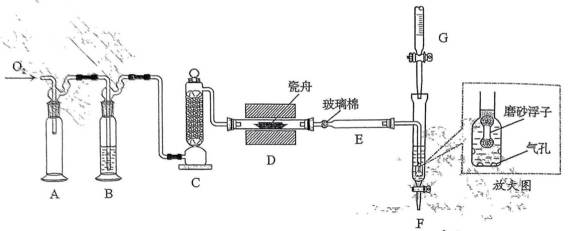
(12分)利用“燃烧—碘酸钾滴定法”测定钢铁中硫含量的实验装置如下图所示(夹持装置略)。
实验过程如下:
①加样,将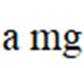
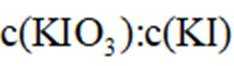
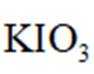
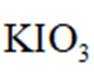
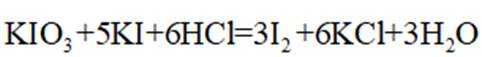
②燃烧:按一定流速通入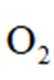
③滴定:当F内溶液浅蓝色消退时(发生反应: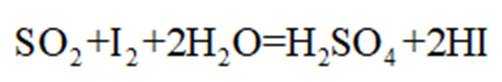
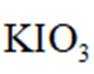
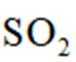
回答下列问题:
(1)取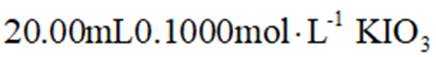
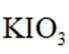
删除A.玻璃棒 B.1000mL锥形瓶 C.500mL容量瓶 D.胶头滴管
(2)装置B和C的作用是充分干燥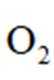
(3)该滴定实验达终点的现象是__________________;滴定消耗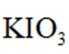
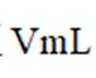
(4)若装置D中瓷舟未加盖,会因燃烧时产生粉尘而促进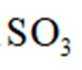
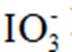
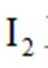
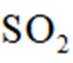
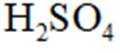
正确答案
(1)AD
(2)浓硫酸 防止发生倒吸
(3)滴入最后半滴标准液溶液,溶液原色变浅蓝色且半分钟内不褪色
(4)催化剂 加热导致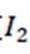
解析
注意20ml稀释倒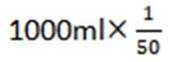
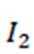
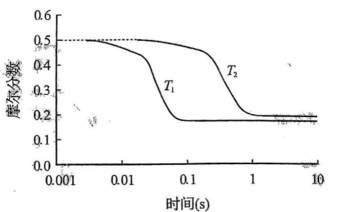
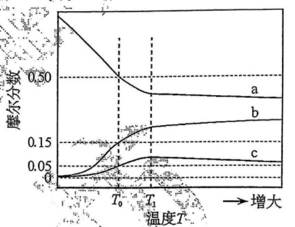
(12分)水煤气是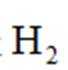
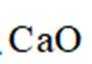
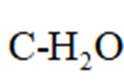
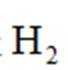
回答列问题:
(1)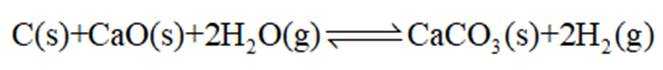
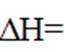
(2)压力p下,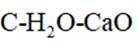
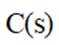
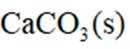
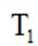
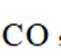
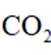
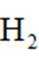
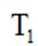
(3)压力p下、温度为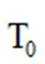
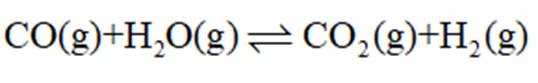
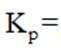
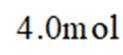
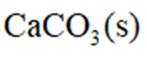
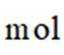
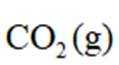
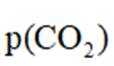
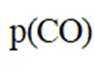
正确答案
(1)
(2)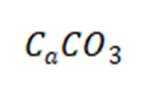
(3)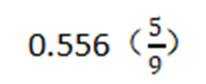
(4)不变 不变
解析
(2)a: