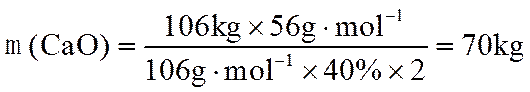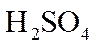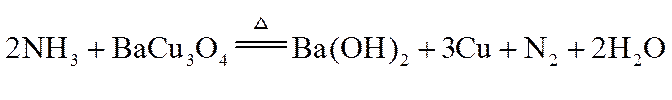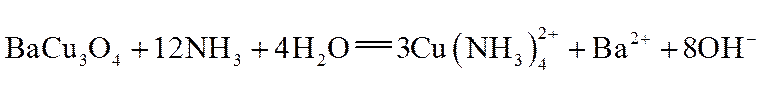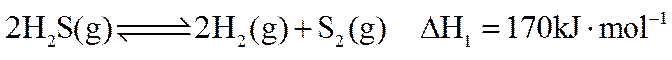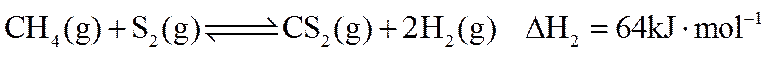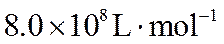- 真题试卷
- 模拟试卷
- 预测试卷
下列消毒剂的有效成分属于盐的是( )
正确答案
下列物质属于强电解质的是( )
正确答案
名称为“吸滤瓶”的仪器是( )
正确答案
下列物质对应的化学式正确的是( )
正确答案
下列表示正确的是( )
正确答案
下列说法不正确的是( )
正确答案
下列说法不正确的是( )
正确答案
下列说法不正确的是( )
正确答案
下列说法正确的是( )
正确答案
关于反应
正确答案
下列说法不正确的是( )
正确答案

正确答案
下列反应的离子方程式不正确的是( )
正确答案
下列说法不正确的是( )
正确答案
染料木黄酮的结构如图,下列说法正确的是( )
正确答案
X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其周期数,
正确答案



正确答案
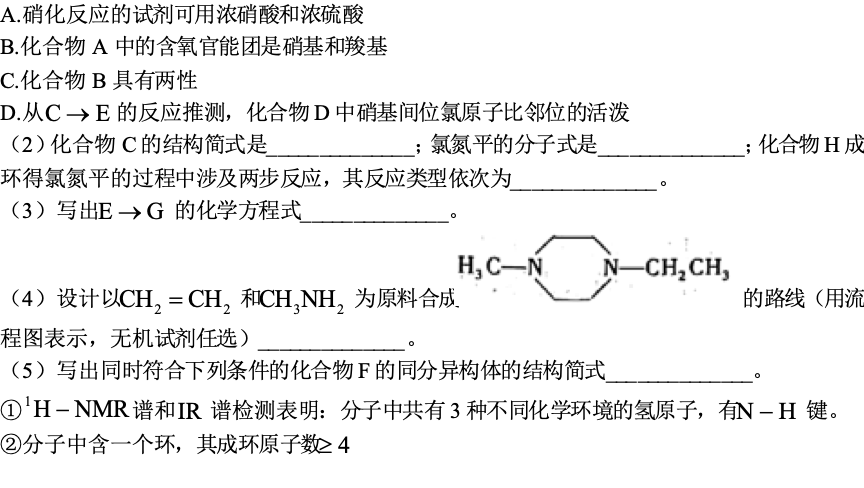
标准状态下,下列物质气态时的相对能量如下表:
可根据


正确答案
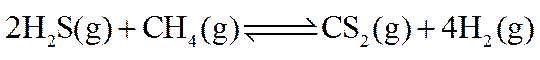
关于反应
正确答案
恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:

正确答案
通过电解废旧锂电池中的


正确答案
关于化合物
正确答案










正确答案
尖晶石矿的主要成分为










正确答案
亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将适量某样品(成分为亚硝酸钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、现象和结论都正确的是( )
正确答案
(1)乙醇的挥发性比水的强,原因是______________。
(2)金属氢化物是应用广泛的还原剂。

正确答案
(1)乙醇分子间形成氢键的数量比水分子间形成氢键的数量少,分子间作用力小
(2)




联合生产是化学综合利用资源的有效方法。煅烧石灰石反应:
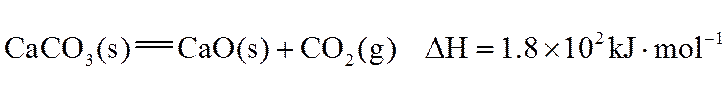
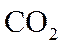
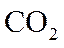
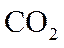
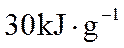
请回答:
(1)每完全分解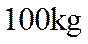
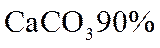
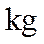
(2)每生产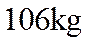
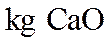
正确答案
(1)10.8
(2)70
由(1)计算可知参与反应的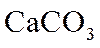
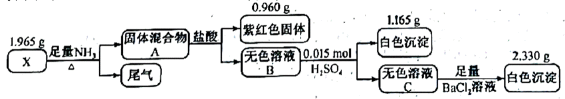
化合物由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到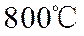
请回答:
(1)组成X的三种元素为______________;X的化学式为______________。
(2)溶液C的溶质组成为______________(用化学式表示)。
(3)①写出由X到A的化学方程式______________。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式______________。
(4)设计实验,检验尾气中相对活泼的2种气体______________。
正确答案
(1)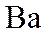
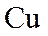
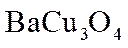
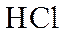
(3)①
②
(4)将湿润的红色石蕊试纸置尾气出口,若变蓝,说明尾气中有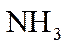
主要成分为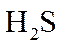
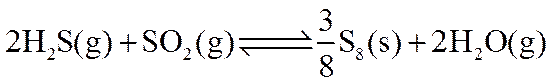
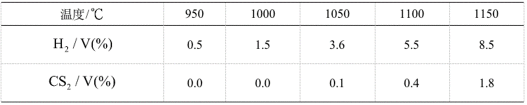
(1)回收单质硫。将三分之一的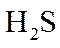
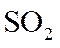
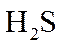
在某温度下达到平衡,测得密闭系统中各组分浓度分别为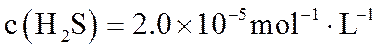
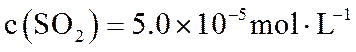
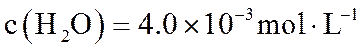
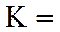
(2)热解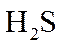
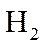
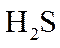
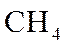
Ⅰ
Ⅱ
总反应:
Ⅲ
投料按体积之比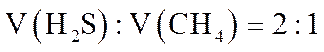
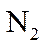
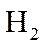
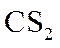
请回答:
①反应Ⅲ能自发进行的条件是______________。
正确答案
(1)
(2)①高温 ②AB
③
④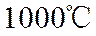
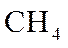
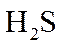
⑤先升后降。在低温段,以反应Ⅰ为主,随温度升高,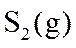
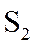
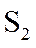
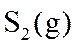
氨基钠(
简要步骤如下:
Ⅰ.在瓶A中加入

Ⅱ.加入

Ⅲ.除去液氨,得产品
已知:
请回答:
(1)
(2)步骤Ⅰ,为判断密闭体系中空气是否排尽,请设计方案______________。
(3)步骤Ⅱ,反应速率应保持在液氨微沸为宜。为防止速率偏大,可采取的措施有______________。
(4)下列说法不正确的是______________。
正确答案
(1)催化 防止氧气、水进入密闭体系
(2)试管加满水倒扣于水槽中,M处通入氨气,将N处排出的气体导至试管内。如试管底部出现气泡,则空气尚未排尽;如未出现气泡,则空气已排尽
(3)分批少量加入钠粒;降低冷却液温度;适当增加液氨量
(4)BC (5)bdg
某研究小组按下列路线合成药物氯氮平。
已知:①
②
请回答:
(1)下列说法不正确的是______________。
正确答案
(1)D
(2)

(3)
(4)
(5)